? ? ? 質量控制是為達到質量要求所采取的作業技術和活動,通過監視質量形成過程,消除質量環上所有階段引起不合格或不滿意效果的因素。其目標在于確保產品或服務質量能滿足要求(包括明示的、習慣上隱含的或必須履行的規定)以達到質量要求,獲取經濟效益。對于體外診斷(In VitroDiagnostic,IVD)試劑產品來說,包括新產品在設計開發階段基于市場需求、臨床需要的小樣制備及性能驗證;注冊申報階段批量的樣品試生產;最終的成品包括根據既定的性能指標要求進行的檢驗以及產品上市后的質量回顧在內的各個環節,均影響到產品上市后的安全性和有效性。以上環節中對人、機、料、法、環的具體要求即構成了該產品有關質量控制的基本鏈條。
如何保證待上市的IVD試劑產品的質量?如何對產品上市后的質量進行持續的、可追溯的監控?擬解決以上問題,企業需對產品全生命周期的不同階段進行控制。其中成品檢驗和留樣檢驗是質量控制的整個鏈條中必不可少的重要環節。這些過程控制的失效會直接影響到上市產品的性能指標,影響診斷結果的準確性和可靠性,進而影響臨床輔助診斷質量,同時對醫療機構精準診療、患者安全以及合理用藥/治療也會產生重要影響。
1.有關體外診斷試劑成品檢驗及留樣檢驗的法規要求
新修訂的《醫療器械監督管理條例》(國務院令第739號)[1] 已于2021 年6 月1 日起實施。《新條例》中也進一步強調了質量管理的要求,如:“第三十條 從事醫療器械生產活動應該具備:(二)有能對生產的醫療器械進行質量檢驗的機構或者專職檢驗人員以及檢驗設備”;“第三十三條 醫療器械生產質量管理規范應當對醫療器械的設計開發、生產設備條件、原材料采購、生產過程控制、產品放行、企業的機構設置和人員配備等影響醫療器械安全、有效的事項作出明確規定”;“第三十五條 醫療器械注冊人、備案人、受托生產企業應當保證出廠的醫療器械符合強制性標準以及經注冊或者備案的產品技術要求”以及第八十六條有關罰則條款的第一條就是“生產、經營、使用不符合強制性標準或者不符合經注冊或者備案的產品技術要求的醫療器械”。《醫療器械生產監督管理辦法》(國家食品藥品監督管理總局令第7 號)[2] 第七條也明確要求“從事醫療器械生產,應當具備以下條件:(二)有對生產的醫療器械進行質量檢驗的機構或者專職檢驗人員以及檢驗設備”。
在我國,按照醫療器械管理的體外診斷試劑是指包括在疾病的預測、預防、診斷、治療監測、預后觀察和健康狀態評價的過程中,用于人體樣本體外檢測的試劑、試劑盒、校準品、質控品等產品,可以單獨使用,也可以與儀器、器具、設備或者系統組合使用。IVD試劑產品作為國內醫療器械的重要組成部分,相關法規文件對其質量控制環節也做出了明確要求。
除了上述提到的通用性上層法規文件之外,在實施層面上,國家藥品監督管理局依據IVD試劑的產品特性,陸續出臺了《體外診斷試劑注冊管理辦法》(國家食品藥品監督管理總局令第5 號)[3];《醫療器械生產質量管理規范附錄體外診斷試劑》[4] 和《醫療器械生產質量管理規范體外診斷試劑現場檢查指導原則》[5]。為指導醫療器械生產企業按照經注冊或備案的產品技術要求做好質量管理,總局又組織制定了《醫療器械生產企業質量控制與成品放行指南》[6] 并予以發布。
綜上,一個待上市的IVD產品的質量穩定性需要從產品的最初設計、樣品的穩定試生產、過程檢驗、成品檢驗以及產品上市后的留樣穩定性考察等質量環上的各個環節綜合進行控制并保證,而成品檢驗及留樣產品的穩定性考察即構成了產品全生命周期中有關質量控制的關鍵控制點。
2.成品檢驗的關鍵控制點
成品檢驗是指對完工后的產品進行全面的檢查與試驗,保證成品的性能符合相關要求,保障成品的有效性。成品檢驗是IVD試劑產品上市前質量控制的關鍵步驟,企業應從人員的職責及培訓;設備的安裝、使用及維護;規范性文件的輸出及記錄的可追溯性等方面進行控制。具體來說,成品檢驗的關鍵控制內容可以概括為以下幾點。
第一,企業應配備適當的人力資源,尤其需關注成品檢驗的具體操作人員及最終產品上市前的放行人員。應明確質量管理部門及相關人員的職責、權限,成品檢驗操作應由經任命、具有相關專業知識背景和實踐經驗并經過崗位培訓的人員完成。對于質量負責人及產品放行人,企業應關注其履職能力。
第二,企業應根據具體產品特性及生產規模,設置相適應的檢驗場地,配備與成品檢驗相符合的檢驗設備,并對該設備進行定期能力驗證及日常管理。對于需計量的設備應制定定期計量計劃,保證其計量審核的符合性。對于出廠檢驗涉及多臺設備的應考慮設備間的差異對檢測結果造成的影響。為符合質量體系運行的可追溯性,應保留主要設備的使用記錄及維護保養記錄,保證設備的可適用性。
第三,企業應當根據強制性標準以及經注冊或者備案的產品技術要求、產品交付要求、企業內部控制標準等制定成品檢驗規程。成品檢驗規程應當確定成品需要實施常規控制的驗證/確認/監視/測量/檢驗/試驗程序與要求,確保每批成品都符合接收準則。接收和拒收及其相關處置措施都應予以記錄[6]。
成品的檢驗規程至少應當明確成品的名稱、規格型號、驗證/確認/監視/測量/檢驗/試驗項目和方法、適用的儀器設備和器具、抽樣程序、抽樣方案、接收準則、引用標準/ 引用測量程序和相關記錄等內容。抽樣方案應當具有統計學依據,應當對統計推斷的置信度進行分析,確保抽檢的樣品具有代表性[6]。
成品檢驗規程的內容原則上應當覆蓋已注冊或者備案的產品技術要求中需要常規控制的檢驗項目和檢驗方法。不能覆蓋的,應當在成品檢驗規程中予以說明。必要時,應當給出經過確認的替代解決方案[6]。
總的來說,企業應確保制定的成品檢驗規程、具體作業指導書與法規批件的一致性;作業指導書的可操作性及制定的檢驗規則的合理性。
第四,最終形成的成品檢驗報告應滿足基本的可追溯性要求,報告中應至少包括檢驗用樣本信息、配套試劑及耗材信息、設備信息、操作人員等。每項性能指標的檢測均應保留原始的檢驗記錄,并與檢驗報告中的項目、結果一一對應。
第五,企業應根據產品技術要求等法規批件制定校準物質的溯源程序文件,應關注因使用不同批次的較高級別參考物質賦值可能對產品造成的影響,制定內控的偏差接收標準并保存適用情況下的評價報告及原始記錄。
第六,企業應當建立并實施成品放行程序,明確成品放行條件、放行批準要求。成品放行前至少應當符合以下條件:完成所有規定的工藝流程;規定的批生產記錄完整齊全;所有規定的進貨、過程、成品檢驗、驗證等質量控制記錄完整齊全,結果符合規定要求,檢驗/ 試驗/ 驗證/ 確認人員及其審核、授權批準人員均已按規定簽發記錄[6]。
3.留樣檢驗的若干要求
產品留樣是指生產企業按照規定保存的、用于質量追溯或調查以及產品性能研究的產品樣品,對該類樣品定期進行性能檢驗及質量穩定性回顧評價有助于在醫療器械產品質量追溯、不良事件調查中查找問題、明晰事故責任,也可為確認或修改產品技術指標提供數據支持。
首先,企業應制定留樣管理制度,以明確留樣目的、留樣樣品、留樣觀察要求及留樣比例/ 數量等內容。IVD試劑產品根據產品特性、工藝特點及臨床應用,其留樣目的基本分為三類:用于產品質量追溯;用于產品原材料質量追溯;用于穩定性研究。
用于留樣的樣品應當滿足以下基本要求:樣品必須是經檢驗合格的產品;應當是從成品批次中隨機抽取的、已完成全部生產工序且能夠代表被取樣批次;包裝形式應當與上市銷售的形式一致;應當明確留樣樣品的型號規格。
用于存放樣品的留樣區域應滿足以下基本要求:留樣區域應相對獨立、足夠存放樣品;原則上,存放條件應與成品一致;留樣區域應配備滿足產品質量特性要求的環境監測設備,定期監測并保存相關記錄。
留樣比例/ 數量原則上由企業自行確定,應至少能支持一次質量可追溯檢測。對于特殊用途的留樣,如新工藝研究、有效期延長,應單獨進行留樣,不影響質量追溯檢測。
企業應當根據不同的留樣目的,明確留樣檢驗/ 留樣觀察的頻次/ 周期,一般來說,留樣觀察時間應當不少于產品有效期。對于穩定性研究用留樣,可適當延長留樣觀察時間或增加觀察頻次。企業應當明確留樣檢驗/ 留樣觀察的項目、檢測方法及判定標準,并具備相應的檢驗能力。
留樣檢驗/ 留樣觀察過程應形成相應的記錄,至少包括:留樣臺賬、留樣檢驗/留樣觀察記錄及報告。檢驗/觀察記錄及報告中應明確留樣批號、檢驗/ 觀察日期、檢驗/ 觀察人員及檢驗/ 觀察結果等。
留樣期滿后應當對留樣檢驗/ 留樣觀察報告進行匯總、分析并歸檔,以評價產品質量,考察產品質量的穩定性。檢驗/ 觀察過程中發現檢測項目不合格時,應當依據相關制度進行處理并分析查找不合格原因。對于留樣期滿后、留樣檢驗剩余的樣品,企業應當按照相關制度予以處理,防止留樣樣品的非預期使用。
4.常見問題
結合日常的現場體系核查匯總數據來看,《醫療器械生產質量管理規范體外診斷試劑現場指導原則》[5] 共十一章節,其中涉及“第八章 質量控制”章節的不合格項在日常體系核查中已經占較高比例(見圖1)。
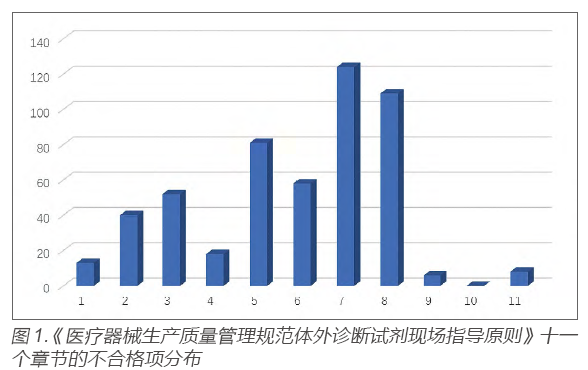
針對第八章的具體條款,不合格項的分布也具有顯著的差異性,主要集中在*8.3.1、8.7.1、8.10.1 等條款上(見圖2)。
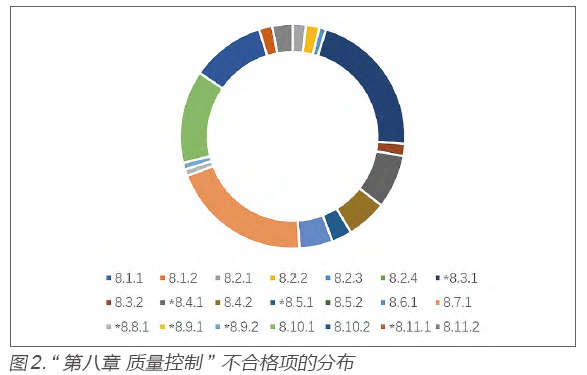
綜上所述,IVD試劑生產企業存在的共性問題可以大致總結為以下幾點。
第一,規范性文件制定的合理性和實際操作的符合性問題,如:成品出廠檢驗規程中的檢驗指標未覆蓋經批準的產品技術要求或檢測方法低于產品技術要求,且未對以上差異進行評估或控制;未制定出廠檢驗或留樣檢驗的檢驗規則;留樣檢驗規程中未明確不同目的留樣的樣品數量、檢驗周期及檢驗內容等;未制定檢驗用企業參考品的配制、定值等過程的作業指導書;產品上市前的實際放行流程與放行相關規定不一致。
第二,具體檢驗記錄的可追溯性問題,如:檢驗報告中未記錄“準確度”檢測使用的企業參考品批號;未記錄“線性范圍”檢測使用的高濃度/ 低濃度血清樣本的信息;未記錄“批內精密度”檢測使用的血清樣品的具體信息(包括:批號、標示值等);參考物質(尤其是企業自制的內部校準品)的臺賬信息不完整(如缺少主要技術指標、溯源途徑等);用于配制檢測用樣品的人源性樣本清單上記錄信息不完整(如樣本原始編號、樣本臨床信息等)。
第三,相關驗證工作的不足,如:目前供采購的國際標準品或國家標準品大多數未明確具體有效期,企業內部一般會自定義其效期,但部分企業缺少相應的驗證性數據支持,如:未制定相關參考物質復驗的周期;企業自定義一級參考品有效期為2 年,但未能提供有效期驗證資料。
5.小結
隨著國內生物醫藥技術平臺的突飛猛進發展,整個國內診斷試劑產業不斷完成技術突破和創新,進口試劑及診斷儀器的壟斷地位正在被民族產品逐步打破,國產IVD試劑產品質量的可靠性和穩定性是拓展廣闊市場前景的基本條件。企業應根據產品特性、方法學平臺、臨床使用的實際需求及法規要求,對不同產品制定合理的成品檢驗及留樣檢驗要求,以確保上市產品的有效性和安全性,并定期進行質量回顧性評價及分析。
參考文獻略
